题目内容:
某温度下,向2L恒容密闭容器中充人1.0 mol A和1.0mol B,发生反应A(g)+ B(g) 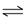 C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
A.反应在前5s的平均速率V(A)=0.15 mol/(L·s)
B.保持其他条件不变,升高温度,平衡时c(A)=0.41mo1· L-1,则反应的△H>0
C.相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的分解率大于80%
D.相同温度下,起始时向容器中充入0.2 mol A、0.2 mol B和1.0 mol C反应达到平衡前反应速率V(正)<V(逆)
参考答案:
