题目内容:
(6分)某同学设计如下实验装置探究“分子的性质实验”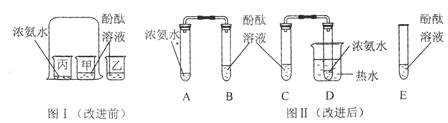
图I是按课本进行的一个化学实验,大烧杯中的实验现象是___________,此实验说明分子______________________。但是在实验时同学们闻到了一股难闻的刺激性气味,于是小明对原实验装置进行了改进,装置如图Ⅱ,并进行如下操作: a. 向B、C、E三支试管中分别加入5 mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色。
b. 在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】(1)E试管放有酚酞溶液的目的是___________。
(2)由此可以得到的实验结论是:①___________,②___________。
(3)对比改进前的实验,改进后实验的优点是___________
参考答案:
