题目内容:
在稀硫酸与锌反应制取氢气的实验中,探究加人硫酸铜溶液的量对氢气生成速率的影响。实验中Zn粒过量且颗粒大小相同,饱和硫酸铜溶液用量0一4.0mL,保持溶液总体积为100.0mL,记录获得相同体积(336 mL,)的气体所需时间,实验结果如图所示(气体体积均转化为标况下)。据图分析,下列说法不正确的是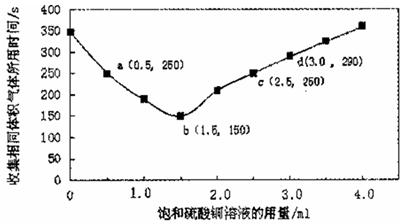 A.饱和硫酸铜溶液用量过多不利于更快收集氢气B.a ,c两点对应的氢气生成速率相等C.b点对应的反应速率为v( H2SO4)=1.0x10-3mol·L -1 ·s-1D.d点没有构成原电池,反应速率减慢
A.饱和硫酸铜溶液用量过多不利于更快收集氢气B.a ,c两点对应的氢气生成速率相等C.b点对应的反应速率为v( H2SO4)=1.0x10-3mol·L -1 ·s-1D.d点没有构成原电池,反应速率减慢
参考答案:
