题目内容:
已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃。某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去)。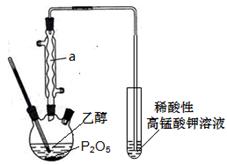

(1)仪器a的名称为_________________
(2)用化学反应方程式表示上述制备乙烯的原理______________________________。
(3)已知P2O5是一种酸性干燥剂,吸水放大量热,在实验过程中P2O5与乙醇能发生作用,因反应用量的不同,会生成不同的磷酸酯,它们均为易溶于水的物质,沸点较低。写出乙醇和磷酸反应生成磷酸二乙酯的化学方程式(磷酸用结构式表示为
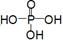 )__________________________________。
)__________________________________。(4)某同学认为用上述装置验证产生了乙烯不够严密,理由是___________________。
(5)某同学查文献得知:40%的乙烯利(分子式为C2H6ClO3P)溶液和NaOH固体混和可快速产生水果催熟用的乙烯,请在上述虚线框内画出用乙烯利溶液和NaOH固体制取乙烯的装置简图(夹持仪器略)。
参考答案:
