题目内容:
NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有:Cu、Zn、Fe、Cr等元素的化合物杂质)为原料获得。有关工艺流程如下: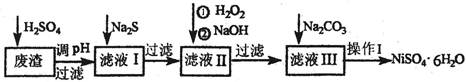
(1)往废渣中加H2SO4酸漫,要充分搅拌,其目的是。
(2)加Na2S的目的是除去铜、锌等杂质,请写出除去Cu2+的离子方程式。
(3)加6%的H2O2时,温度不能过高,其目的是。
(4)除铁方法:用H2O2充分氧化后,再用NaOH控制pH值2~4范围内生成氢氧化铁沉淀。在上述方法中,氧化剂可用NaClO3代替,用NaClO3氧化Fe2+的离子方程式为。
(5)上述流程中滤液III的溶质的主要成分是:。
(6)操作I包括以下过程:过滤,用H2SO4溶解,、、过滤、洗涤获得产品。
参考答案:
