题目内容:
某研究小组为了探究铁合金的生锈情况,设计完成了如下实验,请回答相关问题(I)为探究铁合金生锈的条件,他们用3支试管和3颗铁钉以及相关试剂设计了如下实验装置
 (1)装置Ⅰ中所用蒸馏水应先煮沸冷却后再使用,煮沸的目的是____________________;蒸馏水上层的物质A可以用______________________。
(1)装置Ⅰ中所用蒸馏水应先煮沸冷却后再使用,煮沸的目的是____________________;蒸馏水上层的物质A可以用______________________。(2)装置Ⅱ中试管底部的固体物质B可以用_________________,作用是____________________。
(3)放置一周后,3个装置中只有第Ⅲ个装置中的铁钉生锈了,说明铁钉生锈的条件是____________。
(II)为探究不同条件下铁合金的生锈情况,他们又设计了如下的实验装置
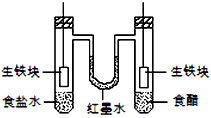 (4)足够长的时间后,装红墨水的U型管中液面情况是_____________________。
(4)足够长的时间后,装红墨水的U型管中液面情况是_____________________。A、左高右低 B、左低右高 C、两边一样高 D、无法确定
(5)装置左边正极反应式为_________________; 装置右边正极反应式为_______________________。
参考答案:
