题目内容:
纳米氧化镁具有特殊的热、光、电、力学和化学等性能,有广泛的应用前景。下图是利用海水制盐的副产品制备纳米氧化镁的流程图。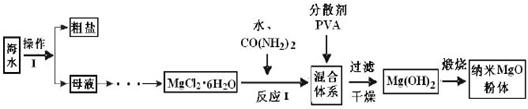
(1)操作I包括蒸发结晶、____________。
(2)操作I后得到的母液中镁离子浓度为1.8×10-3 mol·L-1,要使镁离子产生沉淀,溶液的pH最低应为_____________。(已知:Ksp[Mg(OH)2]= 1.8×10-11)
(3)反应I中CO(NH2)2与H2O反应生成CO2和NH3·H2O,还发生另一主要化学反应的离子方程式为______________________________。
(4)某科研小组研究反应I在378K~398K时的反应时问、反应物的物质的量配比等因素对制备纳米氧化镁产率的影响。请完成以下实验设计表:
实验
编号
T/K
反应
时间/h
反应物的物质的量配比
n[CO(NH2)2]∶n[MgCl2•6H2O]
实验目的
①
378
3
3∶1
(I)实验①和③探究探究反应物的物质的量配比对产率的影响;
(II)实验②和④探究;
(III)实验②和探究反应时间对产
率的影响。
②
378
4
4∶1
③
378
3
④
398
4
4∶1
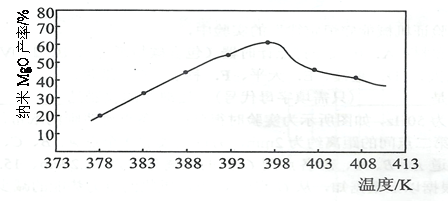
(5)下图为反应的温度对纳米MgO产率的影响。请归纳出温度对纳米MgO产率的影响规律________________________________。
参考答案:
